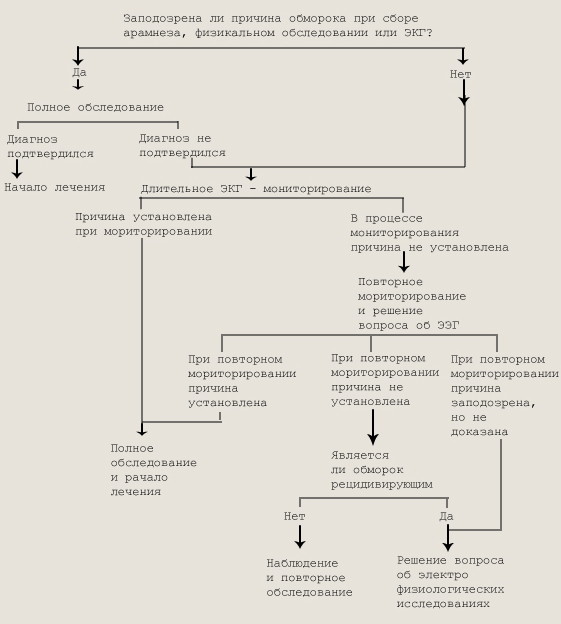
СЕМИОТИКА ПОРАЖЕНИЙ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ Болезни сердечно-сосудистой системы в структуре детской заболеваемости занимают одно из первых мест. За последние годы заметно изменились соотношение, клиническая симптоматика и исход болезней сердца у детей. На первый план выступают неревматические заболевания сердца вирусно-бактериальной природы, имеется тенденция к увеличению частоты врожденных пороков сердца, нарушений ритма и проводимости, а также артериальных гипер- и гипотензий. Для диагностики заболеваний сердца важнейшее значение имеют знание анатомо-физиологических особенностей сердечно-сосудистой системы у детей, анализ анамнестических данных и жалоб больного, данные объективного обследования и лабораторно-инструментальных методов исследования. АНАТОМО-ФИЗИОЛОГИЧЕСКИЕ ОСОБЕННОСТИ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ У ДЕТЕЙ. Закладка сердца начинается на 2-й неделе внутриутробного развития из двух самостоятельных сердечных зачатков, которые затем сливаются в одну трубку, расположенную в области шеи. Она закреплена вверху артериальными стволами, внизу — развивающимися венозными синусами. Вследствие быстрого роста в длину на 3-й неделе трубка начинает изгибаться в виде буквы S, при этом примитивное предсердие и артериальный проток, находившиеся вначале на противоположных концах сердечной трубки, сближаются, а пути притока и оттока смыкаются. На 4-й неделе сердце становится двухкамерным (как у рыб) с клапанами между венозным синусом и предсердием. На 5-й неделе идет образование межпредсердной перегородки и сердце становится трехка-мерным (как у амфибий), на 6—7-й неделе происходит разделение общего артериального ствола на легочную артерию и аорту, а желудочка — на правый и левый. Одновременно формируется проводящая система сердца (с 4-й недели), кроме основных путей (синоатриального, атриовентрикулярного узлов, пучков Гиса, Бахмана, Венкебаха, Тореля) закладываются добавочные (Махайма, Кента, Джеймса и др.). К рождению ребенка происходит инволюция добавочных пучков, и лишь у 0,2—0,1 % детей они остаются. Кровообращение плода. С конца 2-го месяца беременности устанавливается плацентарное кровообращение, сохраняющееся до момента рождения ребенка (до этого возраста зародыш питается гистотрофным способом). Кровь, обогащенная в плаценте кислородом и другими питательными веществами, по непарной пупочной вене в составе пупочного канатика поступает к плоду. Пупочная вена направляется к воротам печени, где образует несколько ветвей, которые сливаются с воротной веной. Печень через эти сосуды получает наиболее богатую кислородом кровь. Другая, большая, часть артериальной крови через венозный проток (аранциев) направляется в нижнюю полую вену и смешивается с венозной кровью, оттекающей от нижних частей тела, печени. Из нижней полой вены смешанная кровь поступает в правое предсердие, куда впадает также верхняя полая вена, несущая венозную кровь из верхней половины тела. В правом предсердии оба потока крови полностью не смешиваются, поскольку кровь из нижней полой вены направляется через овальное окно в левое предсердие, а затем в левый желудочек, тогда как кровь из верхней полой вены устремляется через правое предсердие в правый желудочек. В левое предсердие поступает также небольшое количество крови из легочных вен нефункционирующих легких, это смешение не оказывает существенного влияния на газовый состав крови левого желудочка. При систоле же-лудочков кровь из левого желудочка через aorta ascendens поступает в сосуды, питающие верхнюю половину тела (аа. anonyma, carotis, subclavia sin.), из правого — в легочную артерию; незначительный объем (около 10 %) крови проходит через нефункционирующие легкие и по легочным венам возвращается в левое предсердие. Большая часть смешанной крови из легочной артерии поступает через боталлов (артериальный) проток в нисходящую часть аорты ниже места отхождения больших сосудов, питающих мозг, сердце, верхнюю часть тела. Из нисходящей аорты кровь поступает в сосуды нижней половины тела, относящиеся к большому кругу кровообращения. Частично эта кровь через пупочные артерии поступает обратно в плаценту, где обогащается кислородом, питательными веществами, и вновь поступает через пупочную вену к плоду. Таким образом, для фетального кровообращения характерны: 1) наличие связи между правой и левой половиной сердца и крупными сосудами — два право-левых шунта; Кровообращение новорожденного. При рождении ребенка легкие расправляются и наполняются кровью, фетальные кровеносные пути (аранциев и артериальный протоки, овальное окно и остатки пупочных сосудов) закрываются и постепенно обли-терируются. У новорожденных устанавливается внеутробное кровообращение, начинают функционировать малый и большой круги кровообращения. В левом предсердии возрастает давление крови из-за поступления большого ее количества, и клапан овального окна механически закрывается. Принято считать, что закрытие артериального (боталлова) протока происходит под влиянием нервных, мышечных и торсионных факторов. Обычно к 6-й неделе жизни закрывается артериальный (боталлов) проток, к 2—3 мер — венозный (аранциев) проток, к 6—7 мес — овальное окно в межпредсердной перегородке. Вследствие выключения кровотока через плаценту общее периферическое сопротивление почти удваивается. Это в свою очередь ведет к повышению системного артериального давления, а также давления в левом желудочке и предсердии. Одновременно происходит постепенное значительное (примерно в 4 раза) снижение гидростатического сопротивления в малом круге кровообращения из-за повышения напряжения кислорода в тканях легких (особенностью гладкой мускулатуры сосудов малого круга кровообращения является ее сокращение в ответ на гипоксию) до 15—20 мм рт. ст. к 1—2-месячному возрасту. Следствием снижения сопротивления сосудов малого круга кровообращения является увеличение объема протекающей через них крови, а также снижение систолического давления в легочной артерии, правом желудочке и предсердии. Таким образом, сердце новорожденного обладает большой запасной силой: 1) уменьшение вязкости крови за счет снижения количества эритроцитов; Сердце ребенка имеет ряд анатомо-физиологических особенностей. У новорожденных сердце относительно большое и составляет 0,8 % от массы тела (около 22 г), а у взрослых — 0,4 %. Правый и левый желудочки примерно равны, толщина их стенок составляет 5 мм. С возрастом происходит нарастание массы сердца: к 8 мес масса удваивается, к 3 годам — утраивается, к 6 годам увеличивается в 11 раз. Особенно интенсивно в связи с большей нагрузкой на него растет левое сердце, толщина стенки левого желудочка достигает к 14 годам почти 10 мм (правого — 6 мм). Оба предсердия большие, толщина их стенок 2 мм. Одновременно происходит тканевая дифференцировка. Гистологически миокард новорожденного имеет очень тонкие мышечные волокна, слабо развиты соединительная ткань, продольная фибриллярность и поперечная исчерченность. Ядра представлены в большом количестве, но они мелкие, малодифференцированные. Хорошо развита сеть мелких артерий, которые обеспечивают хорошее кровоснабжение сердечной мышцы. Магистральные сосуды имеют относительно большие размеры. До 10—12 лет у детей легочная артерия шире аорты, затем просветы их становятся одинаковыми, а после полового созревания устанавливается обратное взаимоотношение. Суммарные просветы артерий и вен большого крута кровообращения в раннем возрасте близки между собой (1:1), у детей старшего возраста это соотношение равно 1:3, у взрослых — 1:5. Система капилляров у детей относительно и абсолютно шире, чем у взрослых, что вызывает затруднения в поддержании температурного гомеостаза. У новорожденных особенно интенсивно снабжается кровью головной мозг (39 % МОК и 15 % — у взрослого) и печень (23 % и 30 % соответственно), относительно слабее — скелетные мышцы (< 10 % и 20 %) и почки (12 % и 25 % соответственно). С возрастом увеличивается кровоток через скелетные мышцы и почки, а доля минутного объема крови, протекающей через сосуды мозга, уменьшается. Своеобразие кровоснабжения мозга детей раннего возраста определяется наличием родничков, сглаживающих колебания давления в полости черепа, особенно при крике. Анатомически сердце новорожденного расположено выше, чем у детей старшего возраста, что частично обусловлено более высоким стоянием диафрагмы. Большая ось сердца лежит почти горизонтально. Форма сердца шарообразная. Левый край его выходит за срединно-ключичную линию, правый — за край грудины. На протяжении первых лет жизни и в подростковом возрасте прбисходит поворот и перемещение сердца внутри грудной клетки, в связи с чем границы его меняются: верхняя постепенно опускается, левая приближается к срединно-ключичной линии, правая — к краю грудины. Пульс у детей всех возрастов более частый, чем у взрослых. Это объясняется более быстрой сокращаемостью сердечной мышцы в связи с меньшим влиянием блуждающего нерва и более интенсивным обменом веществ. Повышенные потребности тканей растущего организма в крови удовлетворяются относительным увеличением минутного объема сердца. Частота пульса У детей с возрастом постепенно уменьшается. Крик, беспокойство, повышение температуры тела всегда вызывают у детей учащение пульса. Артериальное давление у детей тем ниже, чем младше ребенок. У новорожденного ребенка систолическое давление составляет в среднем около 70 мм рт. ст., к году оно увеличивается до 90 мм рт. ст. Рост давления в дальнейшем происходит более интенсивно в первые 2—3 года жизни и в пубертатном периоде. Повышение давления с возрастом идет параллельно росту скорости распространения пульсовой волны по сосудам мышечного типа и связано с повышением их тонуса. С возрастом увеличивается удельное периферическое сопротивление за счет: 1) увеличения длины резистивных сосудов и извилистости капилляров: Артериальное давление (АД) у детей измеряется тонометром или сфигмоманометром, размер манжеток зависит от возраста ребенка (ширина манжетки должна составлять примерно 2/3 окружности плеча). У детей первого года жизни давление можно рассчитать по формуле: 76 + 2 п, где 76 — максимальное давление у новорожденного; п — число месяцев жизни. У детей старше года ориентировочно максимальное АД определяется по формуле И.М. Воронцова: 90 + 2 п, где п — возраст ребенка в годах. Минимальное АД составляет 1/2—2/3 максимального. Для измерения АД на ногах манжетка накладывается на нижнюю треть бедра, а стетоскоп прикладывается к подколенной ямке. У здоровых детей АД на нижних конечностях на 5—15 мм рт. ст. выше, чем на верхних. Если при измерении АД «коротковские» тоны сохраняются в процессе понижения давления до нуля (феномен «бесконечного тона»), то диастолическое АД в этом случае определяется в момент резкого приглушения тонов Короткова (четвертая фаза). Принято отсчет АД делать по ближайшей четной цифре. Суммируя все сказанное об анатомо-физиологических особенностях сердечно-сосудистой системы у детей, можно сказать, что относительно большая масса сердца, относительно более широкие отверстия сердца и просветы сосудов являются факторами, облегчающими циркуляцию крови у детей. Для детей раннего возраста характерны малый систолический объем крови и высокая частота сердцебиений, а минутный объем крови на единицу массы тела относительно велик. Относительно большее количество крови и особенности энергетического обмена у детей заставляют сердце выполнять работу, относительно большую, чем работа сердца взрослого человека. Резервные же возможности сердца в раннем возрасте ограничены из-за большей ригидности сердечной мышцы и короткой диастолы, высокой частоты сердечных сокращений. «Преимуществом» детского сердца является отсутствие отрицательного воздействия на сердечную мышцу хронических и острых инфекций, различных интоксикаций. Основные особенности ЭКГ у детей: 1) чем ребенок младше, тем в большей степени преобладает правый желудочек; СЕМИОТИКА БОЛИ В ОБЛАСТИ СЕРДЦА (КАРДИАЛГИИ). Боли в области сердца у детей являются одной из частых причин обращения к врачу. Врачу важно уточнить их локализацию, время появления, постоянство или спорадичность болезненных явлений, интенсивность, распространение, связь боли с физической или психоэмоциональной нагрузкой и другими факторами. Важно установить вызывающие и облегчающие боль факторы. Связанные с поражением сердца кардиалгии у детей наблюдаются при аномальном коронарном кровообращении, перикардитах, при резком расширении сердца или магистральных сосудов. При аномальном коронарном отхождении левой коронарной артерии от легочной (синдром Бландта—Уайта—Гарленда) боли сдавливающие, сжимающие, локализующиеся за грудиной, могут иррадиировать в шею, челюсти, плечи. Боль кардиального генеза всегда ощущается как стенокардическая, однако инфаркт миокарда в юношеском возрасте наблюдается редко. Кардиалгии при поражении миокарда обусловлены нарушением коронарного кровотока в субэндокардиальных отделах сердца или раздражением нервных окончаний вследствие различных причин (воспаление, метаболические сдвиги, ишемия): кардита, кардиомиопатий, гипертрофии миокарда, мио-кардиодистрофии, врожденных пороков сердца и др. Кардиалгии наблюдаются при поражении крупных сосудов — прежде всего при первичной легочной гипертензии, развитии аневризмы при патологии аорты (синдром Марфана, неспецифический аортоартериит и др.), тромбоэмболии легочной артерии и др. Как причина кардиалгии поражение коронарных сосудов в детском возрасте встречается редко и наблюдается при аномалиях коронарных сосудов, при врожденных пороках сердца (тетрада Фалло, стеноз аорты, ее транспозиция, аномальное отхождение левой коронарной артерии от легочной артерии), при коронаритах на фоне СКВ, неспецифического артериита, узелкового периартериита, ЮРА, ревматизма, при неревматических кардитах, инфекционном эндокардите. Относительный дефицит сосудов (коронарные нарушения при гипертрофии) наблюдается при врожденных пороках сердца, кардиомиопати-ях, других состояниях, сопровождающихся гипертрофией миокарда. Боль при этом характеризуется типичной ангинозной симптоматикой — имеет сжимающий, сдавливающий характер, локализуется за грудиной и иррадиирует в левую сторону плечевого пояса. Боль сохраняется в течение длительного времени. Посткардиотомический синдром. Тупая боль за грудиной, лихорадка, артралгии появляются через несколько недель после операции, сопровождающейся вскрытием полости сердца, у 30 % оперированных детей. Характерны расширение границ сердца, увеличенная СОЭ, повышение антител к мышце сердца в крови, что рассматривается как гиперергическая реакция организма на повреждение клеток сердечной мышцы. При перикардите могут быть два вида боли. Плевральная боль, связанная с дыхательными движениями и усугубляемая кашлем и (или) глубоким вдохом, обусловлена плевритным компонентом инфекционного плевроперикардита. Второй тип перикарди-альной боли представляет собой давящую загрудинную боль, имитирующую инфаркт миокарда или стенокардию. Обусловлена боль воспалением чувствительной внутренней париетальной поверхности перикарда или раздражением афферентных нервных волокон сердца, лежащих в периадвентициональном слое поверхностных коронарных артерий. Боль, обусловленная перикардитом, обычно выражается чувством давления. Она возникает при инфекционном или ревматическом перикардите. Интенсивность боли варьирует от незначительной до резкой, боль усиливается при движении, глубоком вдохе. При переходе сухого перикардита в экссудативный болевые ощущения прекращаются, одновременно появляются приглушение тонов сердца, венозный застой, треугольная тень средостения. Тупые продолжительные боли в области сердца, иногда с ощущением сильного покалывания, а также боли, отдающие в левую руку и плечо, как при грудной жабе, могут быть обусловлены миокардитом или перикардитом вследствие острого расширения сердца. Если боли сочетаются с шумом трения, синхронным с ударами сердца, видимым венозным застоем в венах шеи и гепатомегалией, следует думать о перикардите (характерна рентгенологическая конфигурация сердца). Колющая боль в области сердца у юношей. Мальчики жалуются на упорную, длящуюся часами тупую боль в области сердца или на боль в зоне верхушки сердца. Боль может иррациировать в плечо, сопровождаться гипервентиляцией, усиленным вдохом (невозможность полностью вдохнуть), ощущением усиленного сердцебиения, чувством страха. Это может быть связано с невропатической гипервентиляцией (синдром Да Косты, синдром Эффорта). ЭКГ при этом нормальная с высокими зубцами Т, наблюдаются значительные колебания АД со склонностью к психогенным гипертоническим кризам. В отличие от истинной стенокардии эта боль всегда появляется в состоянии покоя на фоне ваготонии, у больных, отличающихся чувствительной и лабильной психикой. Боль при неврозах обычно локализуется в области самого сердца (в области верхушки), бывает колющего, ноющего характера, сопровождается рядом эмоциональных проявлений, двигательным беспокойством. Резкие боли при вдохе, кашле или других дыхательных движениях обычно указывают на плевру и околосердечную область или средостение в качестве возможного источника боли, хотя на боль в грудной стенке, вероятно, также оказывают влияние дыхательные движения. Подобно этому боль, которая регулярно возникает при быстрой ходьбе и исчезает через несколько минут после остановки, по-прежнему считается типичным признаком стенокардии, хотя подобные явления могут отмечаться у больных с нарушениями и повреждениями скелета. Причинами кардиалгии могут быть также патологии позвоночника (нарушение осанки, остеохондроз, травма позвоночника и др.), в основе этих болей лежит особенность иннервации сердца, осуществляемой из спинальных симпатических узлов от трех шейных (С5—С8) и 5—6-го грудных сегментов (повреждение этих областей, особенно шейного отдела, является причиной сердечной дисфункции). ОБМОРОК (СИНКОПЕ) — кратковременная утрата сознания, протекающая с потерей постурального тонуса. Обморок относится к распространенным симптомам, около 30 % здоровых детей сообщают по меньшей мере об одном и более эпизодах потери сознания в течение жизни. Обморок следует отличать от других состояний, протекающих с нарушением сознания: эпилепсии, комы, головокружения вестибулярной природы, нарколепсии, внезапного падения и головокружения невестибулярной природы. Причины обморока можно разделить на связанные с сердечно-сосудистыми заболеваниями, не связанные с сердечно-сосудистыми заболеваниями и неустановленные. Обмороки, связанные с сердечно-сосудистыми заболеваниями, могут возникать при снижении сердечного выброса или нарушении ритма сердца. К заболеваниям, приводящим к уменьшению сердечного выброса, относятся аортальный стеноз, стеноз легочной артерии, гипертрофическая кардиомиопатия, тетрада Фалло, эмболия легочной артерии, легочная гипертензия, мик-сома предсердия, шаровидный тромб, тампонада сердца, расслаивающая аневризма аорты. Выраженная брадикардия и тахикардия могут уменьшить сердечный выброс до возникновения артериальной гипотензии и обморока, в частности нарушения сердечного ритма по типу пароксизмальной тахикардии и приступов Морганьи—Адамса—Стокса, нарушения внутрипредсер-дной проводимости с удлиненным интервалом Q—Ти склонностью к мерцанию желудочков вследствие врожденных (синдромы Романе—Уорда и Джеруэлла—Ланге-Нилсена с лабиринтной глухотой) и приобретенных (гипокалиемия, гипокальцие-мия, миокардит и др.) причин. Цереброваскулярные заболевания не относятся к распространенным причинам обморока. К расстройствам, которые могут привести к обмороку, относятся церебральные васкулиты, болезнь Такаясу, синдром окклюзии подключичной артерии, преходящий вертебрально-базилярный ишемический приступ. Для постановки диагноза важной является разница в величинах АД и наполнения пульса на обеих руках больного, а диагноз преходящего ишемического приступа ставится в случаях, когда эпизод обморока сопровождается симптомами вертебрально-базиляр-ной ишемии и нет других причин обморока. Обморочное состояние может развиться" без внешнего повода, при резком движении головы при аномалиях сосудов мозга или тромботических процессах в них, что вызывает ограничение притока крови к мозгу, а также рефлекторные воздействия на каротидные синусы. Обмороки, не связанные с сердечно-сосудистыми заболеваниями. Наиболее распространенный вид обморока — вазодепрессорный, или вазовагальный. Возникает в ответ на внезапный эмоциональный стресс или в случаях реального, угрожающего или воображаемого повреждения (боль, вид крови, инструментов, вено-пункция, длительное стояние, ожидание боли и др.), при нахождении ребенка в вертикальном положении и реже — в положении сидя. К вазовагальным обморокам склонны дети с вегетативно-сосудистой дистонией, психоэмоциональной лабильностью. Обычно обморок характеризуется наличием в течение нескольких минут продромальных симптомов в виде слабости, бледности, потоотделения, тошноты, похолодания конечностей, сухости во рту, чувства нехватки воздуха, гипервентиляции. Непосредственно перед обмороком появляются внезапная слабость, резкое побледнение, зевота, холодный пот. Вазовагальный обморок обусловлен гемодинамическим механизмом — снижением церебральной перфузии, вызванным артериальной гипотен-зией, которая, в свою очередь, обусловлена снижением общего периферического сопротивления сосудов, последнее не компенсируется повышением сердечного выброса. Снижение периферического сопротивления имеет место в скелетных мышцах и других крупных сосудистых бассейнах — брыжеечном, почечном, мозговом. Ситуационный обморок возникает в ответ на отправления нормальных физиологических функций организма: при мочеиспускании, дефекации, кашле, глотании. Кашлевые обмороки возникают у детей в любом возрасте. Раздражение гортани вызывает очень сильные приступы кашля, например при крупе, астме, коклюше. Обморок развивается на высоте кашля, сопровождается резкой бледностью, потерей сознания, мышечной гипотонией. Подобная картина развивается и при очень сильном смехе. У детей старшего возраста эквивалентом кашлевого обморока являются ощущение общей резкой слабости, помрачение сознания и потемнение в глазах. Дети дошкольного возраста указывают на головокружение, «вращение» комнаты, окружающей обстановки. Они могут быть обусловлены длительным эффектом Вальсальвы или стремительным повышением давления спинномозговой жидкости, приводящим к эффекту, подобному внутреннему сотрясению мозга. При кашле происходит падение сердечного выброса и повышение внутричерепного давления, наряду с этим в результате гипокапнии реф-лекторно увеличивается резистентность мозговых сосудов. После окончания приступа самочувствие обычно хорошее, никаких последствий не возникает. Обморок при глотании обусловлен поражением пищевода или быстрым растяжением желудка. Имеются сообщения о возникновении обморока во время мочеиспускания, он возникает среди ночи, во время или непосредственно после опорожнения, нередко без предшествующих симптомов. Есть сообщения об обмороке во время дефекации, механизм его неизвестен. Ортостатический коллапс (нарушение ортостатической регуляции) возникает при длительном стоянии или при резком подъеме из положения лежа. Ортостатическая гипотензия наблюдается при целом ряде клинических ситуаций, протекающих с уменьшением объема циркулирующей крови или венозного возврата (длительное пребывание в постели или в положении стоя, дегидратация, кровотечение, недостаточность надпочечников и др.). Ортостатическую гипотензию могут провоцировать различные фармакологические средства (гипотензивные, диуретики, нитраты, вазодилататоры, блокаторы кальциевых каналов, ле-водопа, производные фенотиазинов, транквилизаторы) и заболевания центральной и периферической нервной системы (заболевания спинного мозга, симпатэктомия, синдром Шая-Дрейджера, патология периферической нервной системы). Повышение чувствительности каротидного синуса может вызвать брадикардию и артериальную гипотензию, которая приводит к обмороку. Брадикардию можно устранить атропином, однако артериальная гипотензия без брадикардии не чувствительна к атропину. Раздражение каротидного синуса возникает при воздействии локальных факторов: закрытой травмы, кровоизлияния под интиму после пункции (артериографии), сдавления увеличенными лимфатическими узлами, а также инфильтраиии или токсического воздействия со стороны окружающих тканей. Дифференциальная диагностика сосудистых обмороков проводится с истерией. В отличие от ортостатических или вазовагаль-ных обмороков при истерии состояние больного в положении лежа не улучшается, обмороки не сопровождаются ушибами и всегда возникают на людях, а при описании их больной не проявляет тревоги и беспокойства. Оценка синкопе начинается с клинического определения пароксизма, которое должно включать: 1. Анализ ситуаций и факторов, провоцирующих синкопе (эмоциональный стресс, переход из горизонтального положения в вертикальное, связь с натуживанием, сдавлением каротидного синуса, приемом лекарственных препаратов, физической нагрузкой и др.). В случае неясной этиологии обморока наиболее важными являются следующие исследования: общего и неврологического статуса, артериального давления, глазного дна, крови (сахар, остаточный азот, КОС), мочи (белок, ацетон, глюкоза, осадок), ликвора, ЭЭГ, рентгенография, сонография и компьютерная томография черепа.
Диагностический поиск при обмороке СЕМИОТИКА ИЗМЕНЕНИЙ АРТЕРИАЛЬНОГО ДАВЛЕНИЯ. Изменения уровня артериального давления часто встречаются в детской практике: в сторону как его повышения (артериальные гипертензии), так и понижения (артериальные гипо-тензии), особенно в пубертатном возрасте. Артериальные гипертензии. Повышение артериального давления у детей и подростков встречается в 5—10 % случаев. Принято различать первичную (эссенциальную) и вторичную артериальные гипертензии. Считается, что артериальная гипертензия у детей в большинстве случаев является вторичной. До пубертатного возраста повышение АД наблюдается чаще всего при заболеваниях почек (около 70 %), эндокринной системы (синдром Иценко- Кушинга, гиперальдостеронизм, тиреотоксикоз, феохромоци-тома и др.), сердечно-сосудистой системы (коарктация аорты, стеноз устья аорты, недостаточность клапанов аорты, открытый боталлов проток) и т.д. Критерии артериальной гипертензии приведены в таблице 34. При артериальной гипертензии АД превышает возрастную норму — 95-ю центиль. Критерии артериальной гипертензии у детей и подростков разных возрастных групп
В пубертатном периоде высокая частота артериальных гипертензии обусловлена прежде всего гормональной перестройкой, при которой большое значение имеет увеличение продукции адреналина и альдостерона. Сохраняют свое значение в генезе гипертензии болезни почек, эндокринной системы и т.д. В большинстве случаев повышение АД у детей выявляется случайно, и необходимы поиски основного заболевания, приведшего к гипертензии. У детей школьного (в препубертатном и пубертатном) возраста артериальная гипертензия чаще встречается при вегетативно-сосудистой дистонии. Обычно у этих детей выражена эмоциональная лабильность, они предъявляют много жалоб: на плохое самочувствие, раздражительность, легкую утомляемость, боли в области сердца, головные боли и т.д. При объективном обследовании выявляются тахикардия, резистентный верхушечный толчок, прослушивается функциональный шум, иногда акцент II тона над аортой. Артериальное давление превышает возрастную норму (95-ю центиль). У детей раннего возраста артериальная гипертензия чаще протекает бессимптомно. Реже она проявляется задержкой физического развития, признаками сердечной недостаточности, одышкой, рвотой, повышенной или пониженной возбудимостью, судорогами. Первичную артериальную гипертензию необходимо дифференцировать с заболеваниями, при которых повышение АД является ведущим симптомом (вторичные гипертензии) — почечной, эндокринной, нейрогенной и сердечно-сосудистой гипертензией. Почечная гипертензия — в детском возрасте наиболее частая форма вторичной гипертензии. Среди ее причин различаются преренальные (стеноз одной или обеих почечных артерий, компрессия одной из почечных артерий опухолью, гематомой, воспалительным процессом, тяжелый стеноз перешейка аорты, синдром Гольдблатта — тяжелая гипертензия при одно- или двусторонней аномалии почечных артерий с гиперальдостеронизмом и гипокалиемией), ренальные (пороки развития почек, хронический и острый гломерулонефрит, острый и хронический пиелонефрит, ГУС, диабетический гломерулосклероз и др.) и постренальные нарушения, сопровождающиеся затруднением оттока мочи и ее задержкой. Диагноз вазоренальной гипертензии можно заподозрить по стабильной гипертензии с преимущественным повышением диастолического давления, резистен-тности к медикаментозной терапии. При физикальном исследовании может быть выявлен систолический шум над областью отхождения почечных артерий. Диагноз подтверждается данными ангиографии почечных артерий, выявляющими характер и степень поражения почечных артерий, аорты и ее ветвей. При сонографии обнаруживаются уменьшение размеров почки на стороне поражения почечных артерий и некоторое расширение чашечно-лоханочной системы. Диагноз паренхиматозных заболеваний почек устанавливается по мочевому синдрому. В диагностике помогают биопсия почек, сонография, экскреторная урография. Артериальная гипертензия эндокринного генеза наблюдается при феохромоцитоме, синдроме Иценко-Кушинга, адреногенитальном синдроме с гипертензией, первичном альдостеронизме (синдроме Конна), синдроме Бартера, гипертиреозе. Гиперальдостеронизм — повышенная секреция альдостерона — может быть обусловлен первичным поражением надпочечников (первичный Гиперальдостеронизм — синдром Конна) или факторами, активирующими ренин-ангиотензинную систему (вторичный Гиперальдостеронизм). Синдром К о н н а вызывается адьдостеронпродуцирую-щей опухолью — аденомой клубочковой зоны или гиперплазией коры надпочечников. В детском возрасте прежде всего следует думать о вторичном гиперальдостеронизме (стеноз почечной артерии, заболевания почек, адреногенитальный синдром). Характерными признаками синдрома Конна являются артериальная гипертензия с гипокалиемией. У больных резко повышено АД, что сопровождается головной болью, головокружением, нарушением зрения. Хроническая гипокалиемия проявляется адинамией (утомляемость, дискомфорт, мышечная слабость, периодические параличи), канальцевой нефропатией (полиурия, никтурия, полидипсия). Диагноз подтверждается высоким уровнем альдостерона и низкой рениновой активностью. При вторичном гиперальдостеронизме уровень ренина в плазме повышен. При адреногенитальном синдроме могут также встречаться «минералокортикоидные» формы гипертонии, но они являются «дексаметазонзависимыми». Гипертензия при синдроме Конна диагностируется по гипо-калиемии, обусловливающей хронические поносы с общей адинамией вплоть до периодических параличей. Другие симптомы — гипернатриемия и гиперхлоремия, замедление роста. Повышенное выделение альдостерона с мочой подтверждает диагноз. Синдром Бартера— гиперплазия юкстагломерулярного аппарата — также характеризуется гиперальдостеронизмом (вторичный гиперальдостеронизм), который нормализуется под влиянием препаратов, тормозящих синтез простагландинов (индометацин). Гиперкортицизм (синдром Иценко-Кушинга и болезнь Иценко-Кушинга) — синдром, развивающийся в результате гиперфункции коры надпочечников, проявляющийся атипичным ожирением («буйволово» ожирение), артериальной гипертензией, остеопорозом, гипергликемией. Причинами гиперфункции могут быть: изменения в гипоталамусе (болезнь Иценко-Кушинга); базофильная аденома передней доли гипофиза; опухоли коры надпочечников (аденома, рак) и другие опухоли АПУД-системы, продуцирующие полипептиды, по строению и действию близкие к АКТГ; длительный прием глюкокоргикоидов (синдром Иценко-Кушинга). Клиническими симптомами повышенной секреции глюкокортикоидов являются: ожирение, замедленный рост, остеопороз, поли-цитемия, снижение толерантности к углеводам. На коже живота, плеч, бедер появляются синюшно-багрового цвета полосы растяжения (стрии). Избыточный синтез андрогенов вызывает гир-сутизм, вирилизацию (преждевременное оволосение по мужскому типу), появляются угри. Следствием повышенной секреции альдостерона является высокое АД, которое приводит к изменению сосудов глазного дна, почек, нарушению мозгового кровообращения, гипернатриемии и гиперхлоремии. Вследствие гипокалиемии появляются миокардиодистрофические изменения на ЭКГ, нарастает общая мышечная слабость. Диагноз основывается на характерных клинических признаках и лабораторных данных: высокий уровень кортизола и альдостерона в сыворотке крови и повышенное выведение их с мочой; положительный тест с дексаметазоном, метапироном, основанный на подавлении продукции АКТГ. С диагностической целью используются краниограмма, ЭЭГ и ЭхоЭГ, компьютерная томография, эхография, ангиография, ЯМР. Феохромоцитома — опухоль, секретирующая катехо-ламины (адреналин, норадреналин) и происходящая из хромаф-финных клеток. Чаще источником ее служит мозговое вещество надпочечников, реже — абдоминальная симпатическая цепочка на уровне нижней брыжеечной артерии или ее бифуркации и другие симпатические ганглии. Часто это наследственное заболевание с аутосомно-доминантным типом наследования, нередко ассоциируется с другими синдромами и опухолями (синдром Сиппла, множественный эндокринный аденоматоз, нейромы, ганглионейроматоз и др.). Для феохромоцитомы характерны приступообразные гипертонические кризы, в момент приступа — бледность, тошнота, рвота, боли в животе, могут быть поли-урия и полидипсия. Подтверждается диагноз повышенным уровнем катехоламинов в плазме крови, повышенной экскрецией их и их конечных продуктов с мочой (в норме за сутки выделяется 11—76 нмоль адреналина, 47—236 нмоль норадрена-лина, 15—45 мкмоль ванилил-миндальной кислоты). Топический диагноз устанавливается с помощью ангиографии, ЯМР, эхографии и компьютерной томографии. Диффузный токсический зоб (ДТ3, болезнь Греивса, базедова болезнь) — органоспецифическое аутоиммунное заболевание, проявляющееся повышением продукции тиреоидных гормонов щитовидной железой. Клиническая картина заболевания характеризуется синдромами поражения нервной, сердечно-сосудистой систем, желудочно-кишечного тракта, глазными симптомами, увеличением щитовидной железы. Изменения со стороны нервной системы проявляются жалобами на плохой сон и быструю утомляемость, вегетативными сдвигами (преобладание симпатоадреналовой системы) — потливостью, чувством жара, повышением температуры до суб-фебрильных цифр, тремором пальцев рук, век, языка, повышенной возбудимостью, неустойчивым настроением. Тахикардия является ранним и постоянным признаком заболевания, сохраняется во время сна, нарастает параллельно тяжести заболевания, пульс высокий и быстрый, систолическое АД повышено, диастолическое снижено, тоны сердца усилены, над сердцем прослушивается систолический шум. Синдром желудочно-кишечных расстройств характеризуется «волчьим» аппетитом, не сопровождающимся прибавкой массы тела (напротив, ребенок худеет), появлением жажды, дисфункцией желудочно-кишечного тракта (дискинезия желчных путей, гастроптоз, пи-лородуоденоспазм, поносы), увеличением печени. Офтальмопатия в настоящее время рассматривается как самостоятельное аутоиммунное заболевание с поражением рет-робульбарных тканей и глазодвигательных мышц специфическими антителами и выявляется у 60—70 % детей с ДТЗ. Диагноз устанавливается без особых затруднений при наличии типичных симптомов: экзофтальм, увеличение щитовидной железы, изменение поведения, жалобы на сердцебиение и тахикардию, похудание и др. Уровни тиреоидных гормонов в крови повышены: Т3 более 4,0 нмоль/л, Т4 более 200 нмоль/л. Также повышены уровни тиреоглобулина и тиреоидстимулирующих иммуноглобулинов, коррелирующие со степенью тяжести заболевания. Меньшее значение в диагностике ДТЗ имеют гипохолестеринемия, гиполипидемия, лимфоцитоз, нарушения углеводного обмена по диабетическому типу, изменения ЭКГ. Сердечно-сосудистая гипертензия. Стеноз перешейка аорты как причина гипертензии легко диагностируется по повышению АД на верхних конечностях, в то время как на ногах пульс малый или отсутствует и артериальное давление снижено. Диагноз подтверждается сонографией с допплерогра-фией. Открытый артериальный прото к (боталлов) сопровождается повышением АД из-за увеличения минутного объема крови. Диагноз подтверждается наличием систолоди-астолического шума над основанием сердца, сонографией с доп-плерографией. При недостаточности аортального клапана имеют место повышение только систолического давления с соответствующим увеличением амплитуды и скорый пульс. Диастолический шум над основанием сердца или в точке Боткина-Эрба подтверждает диагноз, как и сонография с допплерографией. Повышение АД при поражении мозга (энцефалите, травме мозга, опухоли) никогда не бывает единственным симптомом и поэтому не представляет диагностической проблемы. Гипертензия как один из симптомов отравления (ртутью, таллием, мышьяком), после исключения наиболее частых причин повышения АД, диагностируется по экскреции с мочой или уровню в крови соответствующих металлов. Артериальные гипотензии (АГипо). АГипо — понижение АД, систолического и (или) диастолического за пределы возрастной нормы. У детей — ниже 5-й центили. Кратковременное и умеренное понижение АД у здоровых детей связано с естественными колебаниями его в зависимости от положения тела, суточного биоритма (с наибольшим снижением в предутренние часы); АД понижается после еды, физического и психического утомления, пребывания в душном помещении и т.д. При нарушениях равновесия в активности нейроэндокринных систем регуляции сосудистого тонуса возникают отклонения в уровне АД в большей степени в сторону его снижения. Понижение артериального давления у детей наблюдается при многочисленных состояниях. Различаются физиологическая и патологическая АГипо. Физиологическая артериальная гипотензия — изолированное снижение АД, которое не сопровождается жалобами и снижением работоспособности ребенка. Она может наблюдаться у спортсменов высокого класса, при адаптации организма к условиям высокогорья, тропическому климату. Физиологическая гипотензия может быть лабильной или транзиторной. При низком АД без других проявлений нужно иметь в виду и артериальную гипотензию, являющуюся конституциональной особенностью у детей с подчеркнутой парасимпатикотонией. Патологическая артериальная гипотензия (первичная артериальная гипотензия, нейроциркуляторная гипотензия) встречается у 4—10 % детей. Может протекать в виде гипотензии с обратимым или стойким (гипотоническая болезнь) течением, с ортостати-ческим синдромом. Симптоматическая гипотензия может быть острой, хронической. Первичная артериальная гипотензия (ПАГипо) — мультифакториальная патология, в развитии которой ведущее значение имеют наследственная предрасположенность, а также экзогенные и эндогенные факторы, способствующие ее реализации. Из других причин следует назвать перинатальную патологию, очаги хронической инфекции, высокий инфекционный индекс (группа часто и длительно болеющих детей), психогении, гиподинамию, нарушение режима дня, умственное переутомление. Клинические проявления ПАГипо вариабельны и многообразны. Большинство жалоб объединяется в гипотонические симптомокомплексы: церебральный, общеневротический, сердечно-сосудистый и желудочно-кишечный. Дети с ПАГипо эмоционально лабильны, что проявляется повышенной обидчивостью, плаксивостью, быстрой сменой настроения, утомляемостью, общей слабостью. Они часто жалуются на головную боль (чаще во второй половине дня) давящего, ноющего характера. Каждый второй ребенок жалуется на головокружение — в основном после сна, при резкой перемене положения тела, продолжительных перерывах в приеме пищи. Кратковременная боль в области сердца, ноющая, реже — колющая, наблюдается при физической нагрузке или общем утомлении. Разнообразие изменений сердечного выброса и периферического сосудистого сопротивления объясняет наличие 3 гемодинамических форм — сердечной, сосудистой и смешанной, — регистрируемых при первичной ПАГипо у детей. Обилие жалоб церебрального характера обусловлено нарушениями мозгового кровотока в виде ан-гиогипотонического, ангиоспастического и смешанного синдромов, в том числе затруднением оттока крови из полости черепа. Для ортостатической АГипо типична потеря сознания в вертикальном положении, если не происходит учащение пульса (асимпатикотония), что наблюдается при тяжелой органной или системной патологии (II тип АГипо). Чаще встречается I тип АГипо — менее тяжелое проявление ортостатической гипотен-зии (симптоматика нарушений в ортостазе возникает только при вставании, развивается быстро, сразу при перемене положения, возможны слабость, головокружение с потерей сознания). Необходимость своевременной диагностики первичной артериальной ги-потензии у детей объясняется следующими факторами: 1) артериальная гипотензия среди прочих функциональных расстройств сердечно-сосудистой системы является самой распространенной причиной снижения физической и умственной работоспособности, требующей коррекции; К симптоматическим артериальным гипотензия м относятся гипотензии у больных с эндокринной патологией (гипотиреозом, болезнью Аддисона, гипофизарной кахексией Симмондса, гиперинсулинизмом (гипогликемией), нефрологической патологией, некоторыми врожденными пороками сердца. Симптоматическая гипотензия может быть острой (шок, сердечная недостаточность), а также возникать как побочное явление на фоне медикаментозной терапии. Из сердечно-сосудистых заболеваний артериальная гипотензия наблюдается при стенозе митрального клапана, аортальном стенозе, сердечной недостаточности, что связано с малым систолическим объемом сердца. Некоторое понижение АД обнаруживается при гипотиреозе (характерное выражение лица, микседема-тозный отек кожи, задержка умственного развития и др.), болезни Дауна, болезни Аддисона (постепенное развитие слабости с тошнотой и рвотой, темная пигментация кожи и слизистых оболочек, понижение основного обмена и др.). СЕМИОТИКА НАРУШЕНИЙ СЕРДЕЧНОГО РИТМА. Аритмии — это любой сердечный ритм, отличающийся от нормального синусового ритма изменениями частоты, регулярности, источника возбуждения сердца, нарушением проводимости. Аритмии разнообразны по происхождению, механизму развития, встречаются во всех возрастных группах, что во многом определяет трудности диагностики и лечебной тактики. Все причины нарушения ритма и проводимости можно разделить на кардиальные, экстракардиальные и сочетанные. К кар-диальным причинам относятся органические заболевания сердца (кардиты, кардиомиопатии, кардиомиодистрофии, врожденные и приобретенные пороки сердца); к экстракардиальным — нарушения иннервации сердца при повреждении ЦНС и вегетативной нервной системы, наследственно детерминированная неполноценность вегетативной регуляции, гуморальное воздействие, психогенные расстройства; к сочетанным — поражение миокарда и возникновение импульсов, идущих к ЦНС из зоны поражения. К возникновению аритмий приводит нарушение условий формирования возбуждения и его проведения в сердце. Современная классификация механизмов аритмий предусматривает выделение аритмий, связанных с нарушением процессов образования импульсов, проведения возбуждения, и комбинированных аритмий. Аритмии, вызванные нарушением образования импульсов. Наиболее часто встречающимся нарушением ритма, связанным с нарушением образования импульса, является экстрасисто-л и я — преждевременное сокращение всего сердца или какого-нибудь его отдела по отношению к основному водителю ритма. Экстрасистолы могут быть синусовыми, предсердными, из АВ-соединения и желудочковыми. Анализ различных характеристик экстрасистолического комплекса позволяет разграничить экстрасистолы по топике. Значительно измененный — расширенный и деформированный — комплекс QRS позволяет диагностировать желудочковую экстрасистолу. Для желудочковых экстрасистол характерны следующие признаки: 1) широкий, необычной конфигурации комплекс QRS, появляющийся раньше очередного сокращения желудочков; Если комплекс QRS не изменен, ставится диагноз суправен-трикулярной экстрасистолы. При расположении измененного (деформация или отрицательная инверсия) зубца Р перед комплексом QRS экстрасистолы, укорочении интервала Р— Q (P—R) ставится диагноз предсердной экстрасистолы. Комплекс QRS может быть нормальным или аберрантным. Интервал между предсердной экстрасистолой и следующим обычным сокращением длиннее, чем интервал между сокращениями при синусовом ритме, почти в два раза, то есть появляется неполная компенсаторная пауза. В редких случаях при позднем появлении предсердной экстрасистолы блокируется выход импульса из синусно-предсердного узла, что сопровождается появлением полной компенсаторной паузы. При отсутствии зубца Рили его расположении вслед за комплексом QRS ставится диагноз атриовентри-кулярной экстрасистолы.
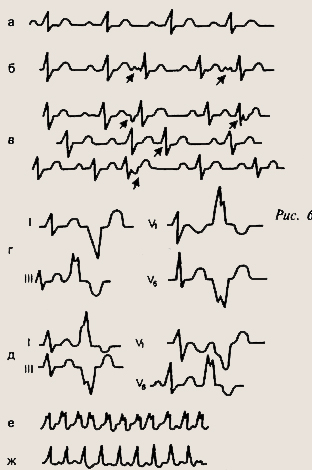
ЭКГ при нарушении возбудимости: а — синусовая аритмия; б — предсердная экстрасистола; в —- экстрасистолы из области атриовентрику-лярного соединения; г — левожелудочковая экстрасистола; д — правожелудочковая экстрасистола; е — желудочковая форма пароксизмальной тахикардии; ж — наджелудочковая форма пароксизмальной тахикардии По времени возникновения по отношению к следующему нормальному сокращению выделяются экстрасистолы сверхранние (возникают на восходящем колене зубца Г предшествующего синусового сокращения), ранние (на нисходящем колене зубца Т или сразу за ним), средние или обычные (начинаются спустя 2—3 с после зубца 7) и поздние (перед предполагаемым зубцом Р следующего обычного сокращения). Экстрасистолы могут быть одиночными, групповыми, возникать в определенном ритме — аллоритмия. По частоте они делятся на редкие (до 5 экстрасистол в 1 мин) и частые (более 5 в 1 мин). Система Лауна предполагает выделение 5 градаций (классов) экстрасистол: 1) монотонные редкие (менее 30 в 1 ч); Экстрасистолы могут возникать у практически здоровых детей (предсердные экстрасистолы у 0,7 %), у больных с хроническими очагами инфекции, при вегетативной дисфункции, у детей с поражениями миокарда, при наличии добавочных пучков проводниковой системы (синдромы предвозбуждения желудочков). Пароксизмальная тахикардия (П Т) инепа-роксизмальная тахикардия (Н Т)являются наиболее частыми видами тахиаритмий у детей, требующими лечения или оказания неотложной помощи. Эти нарушения отличаются механизмами возникновения, началом и продолжительностью. ПТ внезапно начинается после экстрасистолы или в результате синдромов предвозбуждения, приступ длится несколько секунд, минут или затягивается на 2—3 ч, прекращается также внезапно с компенсаторной паузой. Число сердечных сокращений обычно превышает возрастную норму в два раза. Выделяются суправентрикулярная (предсердная и атриовентрикулярная) и желудочковая формы пароксизмальной тахикардии. Основные признаки суправентрикулярной пароксизмальной тахикардии: 1) быстрый (200—300 уд/мин) постоянный ритм; более высокая частота сердечных сокращений наблюдается у детей грудного возраста; Характерные признаки пароксизмальной желудочковой тахикардии: 1) широкие, необычной конфигурации комплексы, как в случае желудочковых экстрасистол; НТ возникает в результате активности гетерогенных очагов автоматизма. Начало медленное, с «разогрева», в конце приступа нет компенсаторной паузы, приступ затягивается на длительное время, число сердечных сокращений до 150—160 уд/мин. При затяжных приступах тахикардии возможно развитие сердечной недостаточности. Уточнение диагноза и определение формы тахикардии проводится на основании ЭКГ-исследования. Мерцательная аритмия. У детей чаще встречается трепетание предсердий (число предсердных сокращений до 300 в 1 мин). В основе заболевания лежат органические изменения в миокарде в сочетании с вегетативной дисфункцией. При мерцании предсердий систола предсердий заменяется сокращением отдельных волокон (свыше 300 сокращений в 1 мин). Различаются брадиаритмическая (число желудочковых сокращений не превышает 60—80 уд/мин) и тахиаритмическая (число желудочковых сокращений более 100 уд/мин) формы. Прогноз зависит от степени миокардиальной недостаточности. При решении вопроса об этиологической дифференциальной диагностике пароксизмальных нарушений ритма следует иметь в виду, что суправентрикулярные формы пароксизмальной тахикардии могут быть как органической, так и функциональной природы. Желудочковая ПТ, фибрилляция и трепетание предсердий практически всегда имеют органическую природу. Пароксизмальные нарушения ритма нередко служат проявлением двух синдромов: преждевременного возбуждения желудочков и слабости синусного узла. Синдром преждевременного возбуждения желудочков возникает в результате того, что синусовый импульс активизирует часть миокарда желудочков не обычным путем, а по более коротким дополнительным проводниковым трактам. Доказано наличие добавочных атриовентрикулярных пучков (Кента), нодовентри-кулярных — от общего ствола пучка Гиса к межжелудочковой перегородке (Махайма), пучка Джеймса, соединяющего предсердия с дистальной частью АВ-узла или пучком Гиса. Преждевременная активация части миокарда желудочков по добавочным пучкам приводит к укорочению интервала Р— R, деформации начальной части комплекса QRS. Эта информация называется волной дельта (А). Она может быть положительной — располагаться на восходящей половине зубца R, высокой или едва заметной — у основания зубца R. Волна дельта может быть отрицательной — имеет вид более или менее уширенного зубца Q или утолщенного отрезка в начале нисходящей части направленного комплекса QS. У детей встречаются два типа синдромов предвозбуждения: WPW-синдром (Wolff-Parkinson-White, Вольффа-Паркинсона-Уайта) и LGL-синдром (Lown-Ganong- Leine, Лауна-Ганонга-Лейна), или CLC-синдром (Clerc—Levy— Cristesco, Клерка-Леви-Кристеско). При проведении возбуждения по добавочному пучку Махайма возникает LGL-синдром. При проведении возбуждения по другим добавочным пучкам возникает WPW-синдром. В зависимости от того, каким путем осуществляется преждевременное возбуждение желудочков, выделяются несколько типов WPW-синдрома. Если импульс проводится по пучкам Кента, возникает типичный классический WPW-синдром, который характеризуется следующими электрокардиографическими признаками: интервал Р— R укорочен (<0,12 с), выражена волна дельта, комплекс QRS уширен. Уширение комплекса QRS компенсирует укорочение интервала Р— R, поэтому расстояние от начала зубца Р до конца R всегда менее 0,2 с. Интервал S— Т и волна Т смещены дискордантно. Если импульс распространяется по добавочному пучку Махайма, на ЭКГ регистрируется нормальный или укороченный интервал Р—R, волна дельта выражена незначительно. Импульс может распространяться одновременно по 2 пучкам: Кента и Джеймса (интервал P—R короткий, желудочковый комплекс незначительно уширен, волна дельта мало выражена), Джеймса и Махайма (интервал Р— R укорочен, волна дельта выражена незначительно). Выделяются несколько ЭКГ-вариантов WPW-синдрома. Тип А — при этом варианте преждевременным возбуждением охватываются волокна заднебазальной части левого желудочка. Волна дельта и желудочковые комплексы положительны во всех грудных отведениях, в отведениях II, HI, aVF волна дельта отрицательна. Тип А у детей встречается редко. Тип В — преждевременное возбуждение переднебазальной части правого желудочка. Комплекс QRS и волна дельта отрицательны в отведениях V, г (форма QS, Qs, rS), в I, II, V5_6 отведениях комплекс QRS и волна дельта положительны. При преждевременном возбуждении заднебазальной части правого желудочка регистрируется тип В WPW-синдрома, но с отрицательной волной дельта только в отведении V,. Может быть смешанный тип — АВ — с признаками обоих типов. Тип С характеризуется отрицательной волной дельта в отведениях V5 и V6. При типе D отрицательная волна дельта регистрируется в отведениях 1, HI, aVF, V,, V4_6. Комплексы QRS в этих отведениях имеют форму QS. У детей эти типы встречаются крайне редко. WPW-синдром может быть постоянным, преходящим, регистрироваться только в отдельных комплексах. При LGL-синдроме на ЭКГ регистрируются короткий интервал P—R (< 0,12 с), нормальный (без волны дельта) комплекс QRS. Периодически могут возникать приступы реципрок-ной АВ-тахикардии. Аритмии, вызванные нарушением проведения возбуждения. Проведение импульса может быть прервано в любом участке проводниковой системы. В зависимости от локализации различаются синоаурикулярная, внутрипредсердная, атриовентрикулярная и внутрижелудочковая блокады. Синоаурикулярная блокада характеризуется блокадой или замедлением проведения импульсов из синусного узла к предсердиям. На ЭКГ отмечается выпадение всех элементов (Р, QRS, Т) сердечного цикла. Интервал между сердечными сокращениями равен почти двойному расстоянию R—R, на его месте регистрируется пауза. Синдром слабости синусного узла (СССУ). Выделяются 3 основных типа СССУ: 1) синоаурикулярные блокады и отказ синусного узла; При внутрипредсердной блокаде нарушается проведение импульсов по межпредсердным проводящим путям (например, пучку Бахмана). На ЭКГ отмечается уширение зубца Р(0,\\— 0,12 с и более) выше возрастной нормы в правых и левых отведениях; также оцениваются расщепления, зазубрины этого зубца в одном отведении. При атриовентрикулярной блокаде нарушается проведение импульсов от предсердий к желудочкам, при этом выделяются полная и неполная блокады. При атриовентрикулярной блокаде 1-й степени интервал P—Qудлинен больше возрастной нормы. При блокаде Мобитца 1-го типа на ЭКГ постепенно удлиняется интервал P—Q, желудочковый комплекс Q— Т периодически выпадает (блокада с периодами Венкебаха—Самойлова), после очередного зубца Р отсутствует комплекс Q— Т. При блокаде Мобитца 2-го типа на ЭКГ периодически выпадает комплекс Q— Г при одинаковой величине интервала Р— Q (нормальный или удлиненный). При полной блокаде на ЭКГ отмечается независимая друг от друга деятельность предсердий и желудочков: расстояния между зубцами Р— Р равны, интервалы R—R также равны, но их продолжительность значительно больше, чем Р—Р. Предсердия сокращаются под влиянием импульсов синусного узла. Форма желудочкового комплекса Q— Т определяется местом рождения импульсов (атриовентрикулярное соединение, ножки пучка Гиса и др.). Внутрижелудочковая блокада (блокада пучка Гиса и его разветвлений). Комплекс QRSи зубец Г изменяются в результате асинхронного возбуждения желудочков, связанного с нарушением проведения импульса по ножкам пучка Гиса. На ЭКГ комплекс QRS уширен, увеличен его вольтаж, зубцы зазубрены, зубец Г уширен и имеет дискор-дантное комплексу QRS направление.
ЭКГ при нарушении проводимости: а — синусовый ритм; б — атриовентрику-лярная блокада I степени; в — атриовентрику-лярная блокада II степени; г — атриовентрику-лярная блокада III степени; д — полная атриовет рикулярная блокада; е— синдром Вольффа—Паркинсона— Уайта (WPW-синд-ром); ж— полная блокада правой ножки пучка Гиса; з — неполная блокада правой ножки пучка Гиса; и — полная блокада левой ножки пучка Гиса При полной блокаде правой ножки пучка Гиса на ЭКГ продолжительность комплекса QRS больше 0,1 с; комплекс QRS в отведениях V,_2 имеет вид rSR,, rSrt, RSR, или М-образный; время внутреннего отклонения удлинено до 0,04 с и более; зубец S в отведениях I, V5_6 уширен и часто зазубрен; электрическая ось сердца отклонена вправо; зубец Т и интервал S— Гдискордант-ны конечной части комплекса QRS, сегмент ST снижен, зубец Г отрицательны и в отведениях III, V , сегмент ST приподнят, зубец Т положительный в отведениях I, aVL, V,_6. Для неполной блокады правой ножки пучка Гиса в отведениях V, 2 характерна форма желудочкового комплекса rRp rSRr RSRr длительность комплекса QRS не превышает возрастной нормы. Полная блокада левой ножки пучка Гиса на ЭКГ характеризуется следующими признаками: продолжительность комплекса QRS больше 0,1—0,12 с, комплекс QRS в отведениях I, aVL, V5_6 имеет вид rRp в отведениях Vt_2—rS или QS; сегмент ST и зубец Т смещены в направлении, противоположном основному отклонению комплекса QRS, электрическая ось сердца отклонена влево, время внутреннего отклонения в отведениях V._6 более 0,05 с. При неполной блокаде левой ножки пучка Гиса комплекс QRS слегка уширен (не более 0,1 с), электрическая ось сердца отклонена влево, время внутреннего отклонения в отведениях V5_6 более 0,05 с, на восходящей части зубца R имеется излом. При блокаде левой передней ветви пучка Гиса на ЭКГ электрическая ось сердца отклонена влево (от минус 30 до 90°), отмечаются высокий зубец R в отведениях I, aVL и глубокий зубец S в отведениях II, III, aVF, нормальный или слегка уширенный комплекс QRS. Блокада левой задней ветви пучка Гиса на ЭКГ характеризуется отклонением электрической оси сердца вправо при отсутствии признаков гипертрофии правого желудочка или других кар-диальных или экстракардиальных причин, высоким зубцом R в отведениях II, III, aVF и глубоким зубцом S в отведениях I, aVL. Возможны комбинированные нарушения проводимости по правой и левой ножкам, а также ветвям левой ножки пучка Гиса. Периферические, или терминальные, блокады (блокада волокон Пуркинье) у детей практически не встречаются. Комбинированные аритмии. Парасистолия — это нарушение ритма, в основе которого лежит существование двух независимых друг от друга очагов образования импульса. Водителем основного ритма является обычно синусный узел. Эктопический очаг располагается чаще всего в желудочках, очень редко—в АВ-соединении или предсердиях. В зависимости от этого различаются желудочковые, атриовентрикулярные, предсердные парасистолы. Парасистолы могут регистрироваться на фоне мерцательной аритмии, могут сочетаться с желудочковыми экстрасистолами, блокадой ножек пучка Гиса. Чаще всего парасистолы одиночные, изредка трансформируются в желудочковую тахикардию. Электрокардиографическими признаками парасистол являются: 1) непостоянство предэктопического интервала (расстояние между зубцом R парасистолы и R предшествующего нормального сокращения), разница между предэктопическими интервалами в различных сокращениях превышает 0,06 с; Ишемия миокарда, особенно субэндокардиальной области, которая хуже всего снабжается кровью, часто встречается у детей при тяжелой общей гипоксемии, тяжелом стенозе устья аорты и легочного ствола, коронарной недостаточности. Для ишемии миокарда характерны патологическое снижение сегмента ST более чем на 2 мм от исходного уровня при длительности его более 0,08 с либо наклон ST вниз с инверсией зубца Т (снижение сегмента ST или его подъем на 1 мм в стандартных отведениях или на 2 мм в грудных отведениях может наблюдаться у здоровых детей). Аналогичные наблюдаемым при ишемии миокарда изменения сегмента ST могут быть при миокардите, перикардите, тяжелой гипертрофии левого и правого желудочка. Диагностика нарушений ритма. Клинические проявления аритмий неспецифичны, иногда вообще не выражены или проявляются в стертой форме, и диагноз устанавливается лишь на основании данных ЭКГ. Дети чаще всего предъявляют жалобы на сердцебиения, перебои в сердце, чувство «замирания», «остановки» сердца. Важны указания на внезапное начало сердцебиения и такое же внезапное окончание приступа. Предположение о возможности аритмии может возникнуть при приступах головокружений, синкопальных состояниях, наблюдаемых при брадикардии (синусовая брадикардия, синоатриаль-ные блокады, атриовентрикулярные блокады 1—3-й степени). Объективные признаки выявляются при исследовании частоты и характера пульса и аускультации сердца. В частности, изменяются такие свойства пульса, как частота (частый или редкий пульс), ритм (неритмичный), величины пульса (пульсовые волны различной величины), определяется дефицит пульса — не все пульсовые волны доходят до периферии. Аускультативно выявляются также нарушения ритма сердечных сокращений, изменение громкости тонов (различная громкость). Многие аритмии могут не влиять на самочувствие ребенка, не обнаруживаются при объективном обследовании и выявляются часто случайно при проведении электрокардиографии. В то же время жалобы на аритмию могут быть субъективными и не сопровождаться какими-либо объективными данными и изменениями ЭКГ. Верификация диагноза аритмии проводится при электрокардиографии (регистрация ЭКГ с длительной записью в отведениях I, Vj и V3, где хорошо регистрируется зубец Р). По показаниям осуществляются регистрация ЭКГ с чреспищеводным и внут-рипредсердным отведениями, холтеровское мониторирование, электрофизиологическое исследование и электрография атрио-нодальной проводящей системы. В ряде случаев для установления генеза аритмий необходимо проведение целого ряда дополнительных исследований: 1) изучение анамнеза, семейной и наследственной отягощен-ности с целью установления возможных причин аритмии; СЕМИОТИКА ШУМОВ СЕРДЦА. Одним из частых признаков поражения сердца являются шумы сердца. У детей они подразделяются на систолические и диастолические, по происхождению могут быть органическими и функциональными. Шумы у детей, как и тоны, выслушиваются более звучно и отчетливо. Различаются по громкости, продолжительности, тембру, зоне максимальной локализации и области преимущественного проведения, связи с систолой или диастолой. Функциональные шумы у детей и подростков
Дифференциально-диагностическая таблица функциональных и органических систолических шумов сердца у детей
Органические шумы могут возникать в систолу и диастолу, характеризуются достаточно определенной и постоянной связью звукового феномена с анатомическим субстратом в виде изменений стенок, отверстий или клапанов сердца или перикарда. К ним можно отнести шумы при приобретенных и врожденных пороках сердца и магистральных сосудов, при воспалении эндокарда и перикарда, звуковой феномен — щелчки и шумы пролапса митрального клапана. Об органической природе шума могут свидетельствовать шумы диастолические, пансистолические, шумы в конце систолы и сочетающиеся с дрожанием, очень громкие шумы, шумы, которые сопровождаются некоторыми нарушениями сердечно-сосудистой системы, — асимметрия пульса, щелчки, патологическое расщепление тонов и др. Систолические шумы делятся на пансистолические, ранние, средние, поздние. Систолический шум возникает при врожденных и приобретенных пороках сердца и сосудов. Диастолические шумы у детей в абсолютном большинстве случаев имеют органический генез и возникают при: недостаточности полулунных клапанов аорты и легочной артерии, стенозе левого и правого атриовентрикулярных отверстий, патологическом сбросе крови в диастолу (дефект аортолегочной перегородки, открытый аортальный проток, общий артериальный ствол при недостаточности клапана трункуса и др.). В отличие от систолических шумов интенсивность диастолических коррелирует с тяжестью порока. Протодиастолический шум характерен для недостаточности полулунных клапанов, мезодиастолический и пресистолические возникают при стенозе предсерд-но-желудочковых отверстий.
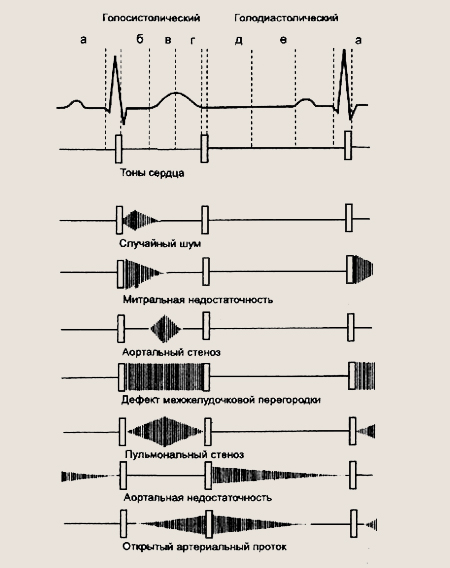
Сердечные шумы (характерный шум позволяет предположить наличие соответствующего порока): а — пресистолический; б — протосистолический; в — мезосистолический; г — поздний систолический; д — протодиастолический; е — мезодиастолический Функциональные шумы могут встречаться у практически здоровых детей в различные возрастные периоды. По пути кровотока, происходящего из системных вен через сердце к аорте, может возникнуть пять нормальных шумов, которые можно определить следующим образом: 1) ш у м «волчка» (соединение яремной, подключичной и безымянной вен с верхней полой веной): непрерывный, часто с диастолической акцентацией; лучше всего выслушивается под правой ключицей; может проводиться в верхнюю часть грудной клетки слева; полностью исчезает в положении лежа, что позволяет дифференцировать его с шумом открытого аортального протока или артериовенозной фистулы; Можно выделить, кроме того, еще несколько групп функциональных шумов у детей. Шумы при вегетативной дисфункции вследствие изменения мышечного тонуса, особенно папиллярных мышц (укорочение или удлинение мышц), что создает условия для неполного смыкания створок клапанов. Чаще такие шумы возникают у подростков, у которых наряду с вегетативной дисфункцией повышена активность щитовидной железы. Шумы формирования сердца возникают вследствие того, что различные отделы сердца растут неравномерно, что обусловливает относительное несоответствие размеров камер и отверстий сердца и сосудов, которое приводит к турбулентности тока крови и возникновению шума. Может иметь место неравномерность отдельных створок клапанов и хорд, что приводит не только к временной несостоятельности запирающей функции клапанов, но и к изменению их резонансных свойств. Эти шумы наиболее часто выслушиваются на легочной артерии у детей преддошкольного и дошкольного возраста, на верхушке — у детей школьного возраста. Шумы мышечного происхождения обусловлены снижением тонуса папиллярных мышц или всего миокарда. Выслушиваются над верхушкой и в точке Боткина. Они чаще являются следствием неполного смыкания створок клапанов и регургитации крови. Причинами этих шумов являются острые или хронические дистрофические изменения миокарда, нарушения обмена в сердечной мышце (мукополисахаридозы, гликогенозы и др.). Шумы«малых»аномалий сердца и сосудов относятся к пограничным шумам. Это обычно нарушение архитектоники трабекулярной поверхности миокарда или своеобразие расположения хорд, строения папиллярных мышц, небольшие отверстия в перегородках, нерезко выраженные стенозы крупных сосудов и др., создающие турбулентность тока крови, вследствие чего возникают шумы. В отличие от органических функциональные шумы занимают ограниченную зону, не проводятся за пределы карди-альной области, нежные по тембру или носят вибрирующий, «струнный» характер. Такие шумы непостоянны, их интенсивность меняется в зависимости от фазы дыхания и положения тела ребенка. Они лучше слышны в положении лежа на спине; в вертикальном положении и после физической нагрузки их интенсивность значительно ослабевает или они вообще исчезают, им свойственна лабильность во времени — исчезновение или усиление при выслушивании через короткие промежутки времени. Условно дети с функциональными (атипичными) шумами могут быть разделены на три группы: 1-я группа — здоровые дети с безусловно функциональным шумом типа шума формирования или шума легочной артерии; СЕМИОТИКА ПОРОКОВ СЕРДЦА. Пороки сердца являются нередкой патологией у детей, и частота их в последние годы увеличивается. Врожденные пороки сердца. Частота врожденных пороков сердца (ВПС) у новорожденных детей составляет 0,8 %, они широко варьируют по анатомическим особенностям и тяжести течения. Благодаря введению в практику новых радикальных и паллиативных хирургических методов лечения значительно повысилась выживаемость этих детей, однако еще большое число их (почти треть) погибает в течение первого года жизни. Особенно высока летальность среди таких детей в первый месяц жизни. С возрастом частота встречаемости различных форм ВПС у детей изменяется, хотя около 85 % от всех ВПС составляют восемь наиболее распространенных пороков, другие пороки встречаются реже. Клинические проявления ВПС у детей разнообразны и определяются тремя основными факторами: анатомическими особенностями порока, степенью компенсации и возникающими осложнениями. ВПС у новорожденного или ребенка первых месяцев жизни можно заподозрить, если у него выявляются: 1) цианоз или выраженная бледность (бледность как аналог цианоза характеризуется повышением гематокритного числа); Окончательный диагноз ВПС устанавливается на основании особенностей клинических проявлений и данных УЗ И сердца, зондирования его полостей. В зависимости от особенностей гемодинамики ВПС разделены на три подгруппы. 1. Врожденные пороки сердца с обогащением малого круга кровообращения. Дефект межпредсврдной перегородки (Д М П П) является одним из распространенных ВПС. Различаются первичные дефекты (Ostium primum), которые по эмбриологическому признаку объединяются в группу пороков развития атриовентрикулярного канала (15 %), и вторичные дефекты перегородки (Ostium secundum) — 70 %. 15 % всех ДМПП локализуется вблизи устья верхней полой вены и синусного узла, реже встречаются множественные дефекты и полное отсутствие межпредсердной перегородки. В 10—20 % случаев ДМПП сочетается с пролапсом митрального клапана. Спонтанное закрытие дефекта в межпредсердной перегородке наблюдается чаще, чем предполагалось ранее. Признаки наиболее распространенных врожденных пороков сердца у детей
Гемодинамика при ДМПП определяется сбросом артериальной крови слева направо, что приводит к увеличению минутного объема малого круга кровообращения. В образовании шунта имеют значение разница давления между правым и левым предсердием, более высокое положение последнего, большая растяжимость правого желудочка и площадь правого атриовентрикулярного отверстия, сопротивление, объем сосудистого ложа легкого. Развитие легочной гипертензии и поражение сосудистого русла легких приводят к обратному шунтированию крови и появлению цианоза. При первичных дефектах часто наблюдается митральная недостаточность. В отличие от дефектов межжелудочковой перегородки, при которых значительный сброс приводит к объемной перегрузке обоих желудочков, при ДМПП сброс крови меньше и влияет только на правые отделы сердца. Симптоматика нередко отсутствует, и порок выявляется лишь при физикальном обследовании. При рождении или в течение первого года жизни порок распознается у 40 % больных, у остальных — обычно в возрасте 2—7 лет. При выраженном сбросе у больных наблюдаются отставание в весе и склонность к повторным респираторным заболеваниям и пневмониям в первые годы жизни. Как правило, в этих случаях имеются жалобы на одышку, утомляемость, боли в сердце. Границы сердца расширены в поперечнике и вправо за счет правых отделов сердца. Выслушивается негрубый систолический шум во втором-третьем межреберье слева от грудины. II тон на легочной артерии усилен, расщеплен. При развитии легочной гипертензии появляется акцент II тона на легочной артерии и может присоединяться диастолический шум Грэма Стилла за счет развития недостаточности клапанов легочной артерии. На ЭКГ выявляются признаки диастолической перегрузки правого желудочка с нормальной или отклоненной вправо ЭОС и частичной или полной блокадой правой ножки пучка Гиса (отсутствие признаков нарушения проводимости ставит под сомнение диагноз ДМПП). Рентгенологически определяется разной степени выраженности увеличение правых отделов сердца. Левый желудочек гипоплазирован, легочные артерии расширены, значительно усилен легочный рисунок. Диагноз подтверждается с помощью эхокардиографии (визуально определяются размер и локализация дефекта, с помощью допплеровского исследования, в том числе цветного картирования, оцениваются величина и направление сброса, рассчитывается давление в легочной артерии) и при необходимости катетеризации сердца. Дефект межжелудочковой перегородки (ДМЖП) является одним из наиболее часто встречающихся ВПС. На его долю приходится от 17 до 30 % случаев сердечных аномалий. Наиболее часто встречаются дефекты в мембраноз-ной части перегородки (75 %). Располагаются в верхней части межжелудочковой перегородки сразу под аортальным клапаном и септальной створкой трехстворчатого клапана, часто закрываются самопроизвольно. Реже (10 %) выявляется дефект в мышечной части перегородки (болезнь Толочинова—Роже). Мышечные дефекты бывают множественными, фенестрированными и часто также закрываются самопроизвольно. Надгребневые (ДМЖП выносящего тракта правого желудочка, 5 %) располагаются выше наджелудочкового гребня, часто сопровождаются аортальной недостаточностью, самопроизвольно не закрываются. Дефект АВ-перегородки (ДМЖП приносящего тракта правого желудочка, 10 %) часто встречается при синдроме Дауна. Самопроизвольно не закрывается. Редко встречаются множественные дефекты МЖП («swiss cheese»). Выраженность шунта слева направо определяется размером дефекта и соотношением сопротивления сосудов малого и большого кругов кровообращения. До тех пор, пока легочное сосудистое сопротивление ниже системного, происходит шунтирование крови слева направо. Если легочное сопротивление превосходит системное (при больших дефектах и высоком легочном сосудистом сопротивлении), направление сброса меняется на обратное (комплекс Айзенменгера). Первым проявлением заболевания обычно служит грубый систолический шум в сердце, который лучше выслушивается в 5-й точке, часто с дрожанием, определяемым при пальпации. Имеется сердечный горб. По мере увеличения легочного сосудистого сопротивления систолический шум становится короче, а легочный компонент II тона — интенсивнее. Выделяются три типа развития ДМЖП в зависимости от особенностей гемодинамики порока (величины лево-правого шунта), определяющих клинические проявления и прогноз заболевания. Первый тип — имеется маленький дефект в перегородке (менее 0,5 см2/м2), малый сброс крови (< 25% ударного объема) не вызывает изменений давления в правом желудочке и малом круге кровообращения, легочная гипертензия не развивается. Клинические проявления отсутствуют. Дети с таким пороком не нуждаются в систематическом лечении. Второй тип — средней величины дефект (0,5—1 см2/м2) приводит к большему сбросу крови в правый желудочек (< 50 % ударного объема) и среднему повышению давления в малом круге кровообращения. При этом типе ДМЖП мало выражены клинические признаки порока и не возникает проблем с лечением. Могут наблюдаться отставание в физическом развитии, застойная сердечная недостаточность, рецидивирующие нижнедолевые пневмонии. Оперируют таких детей в дошкольном возрасте. Третий тип — большой дефект (более 1 см2/м2), когда сброс крови в правый желудочек превышает 50 % ударного объема. Характеризуется частыми бронхолегочными заболеваниями, нарушениями роста и признаками сердечной недостаточности, при выраженности которых прибегают к радикальной или паллиативной операции. При высоком легочном сопротивлении (комплекс Айзенменгера) могут наблюдаться одышка в покое и при физической нагрузке, боли в груди, цианоз, кровохарканье. Большинство больных умирает в детском и подростковом возрасте. На ЭКГ возможны признаки перегрузки и гипертрофии левого желудочка, комбинированной перегрузки обоих желудочков или перегрузки правых отделов сердца. Иногда наблюдается нарушение предсердие-желудочковой и внутрижелудочковой проводимости. Рентгенологически чаще отмечается выраженная кар-диомегалия со значительным выбуханием обоих желудочков, левого предсердия и легочной артерии. На эхокардиограмме выявляются признаки объемной перегрузки левых предсердия и желудочка, степень увеличения которых отражает объем шунта справа налево. С помощью допплеровского исследования (в том числе цветного картирования) оценивается величина и направление сброса, рассчитывается давление в легочной артерии. Изменения гемодинамики при ДМЖП выявляются также при катетеризации сердца. Большинство дефектов межжелудочковой перегородки имеют малый размер и представляют риск в отношении инфекционного эндокардита. Открытый аортальный проток (ОАП). Артериальный (боталлов) проток соединяет легочную артерию и аорту непосредственно за левой подключичной артерией. Функциональное закрытие открытого аортального протока у доношенных детей происходит через 10—15 ч после родов, облитерация протока — через несколько недель жизни. У недоношенных детей ОАП может функционировать от нескольких недель до месяца. У доношенных детей он остается открытым при структурных аномалиях, у недоношенных тем чаще, чем более незрелый ребенок, хотя спонтанное закрытие встречается часто. При ОАП наблюдается сброс крови из аорты в легочную артерию из-за более высокого давления в аорте, что приводит к переполнению малого круга кровообращения и перегрузке левых камер сердца. При развитии легочной гипертензии присоединяется перегрузка и правого желудочка. Диаметр и длина протока определяют тяжесть сопутствующих гемодинамических нарушений, которые аналогичны таковым при ДМЖП различных размеров. Кровоток при ОАП происходит как в систолу, так и в диастолу. Объем шунта слева направо и давление в легочной артерии возрастают параллельно с увеличением диаметра сообщения. Если легочное сопротивление превосходит системное, то наступает смена направления шунта. Это наблюдается при больших размерах протока. Обычно клинические проявления порока возникают в конце 1-го или на 2—3-м году жизни. Дети до появления клинических симптомов порока развиваются физически и нервно-психически нормально, а первая фаза течения порока у части из них протекает легко. Ранние клинические признаки порока возникают при широких протоках. Границы сердца расширены преимущественно влево и вверх. Во втором межреберье слева от грудины выслушивается систолодиастолический («машинный») шум, проводящийся на верхушку сердца, шейные сосуды, аорту и в межлопаточное пространство. Шум изменяется в связи с дыханием. Длительность диастолической части шума может быть укорочена у новорожденных и у пациентов более старшего возраста .с легочной гипертензией. Ослабление или исчезновение шума указывает на развитие легочной гипертензии, когда давление в большом и малом круге кровообращения выравнивается. II тон на легочной артерии при этом усилен. На ЭКГ электрическая ось сердца расположена нормально или отклонена влево, отмечаются признаки гипертрофии левого (или обоих) желудочка. При рентгенологическом исследовании выявляется увеличение левых отделов сердца и усиление кровенаполнения легких. Эхокардиография позволяет лоцировать проток и сброс крови из аорты. Полная транспозиция магистральных соусудов (Т М С) — аорта отходит от правого желудочка, легочная артерия — от левого, при этом образуются два отдельных и независимых друг от друга круга кровообращения. Жизнь ребенка после рождения возможна только при наличии компенсирующих коммуникаций (ОАП, ДМПП, ДМЖП). У большинства больных имеется внутрипредсердное сообщение, у 65 % — ОАП, у 35 % — ДМЖП. Этот порок сердца представляет собой основную причину смерти в первые два месяца жизни среди других впс. Порок чаще встречается у мальчиков. С момента рождения наблюдается постоянный цианоз. Границы сердца расширены в поперечнике и вверх. Аускультативная картина нехарактерна, она определяется компенсирующими коммуникациями. Течение тяжелое, прогрессирующее, при клинике сердечной недостаточности большинство детей быстро умирают, если им не проводится оперативное лечение. На ЭКГ электрическая ось сердца смещена вправо, определяются признаки гипертрофии правых отделов сердца. Рентгенологически выявляются кардиомегалия, сужение талии сердца и увеличение легочного кровотока. С помощью допплеровского исследования (в том числе цветного картирования) оцениваются размеры дефектов, величина и направление сброса. 2. Врожденные пороки сердца с обеднением малого круга кровообращения. Стеноз легочной артерии (С Л А) обусловлен чаще стенозом клапанов легочной артерии, реже — под- и над-клапанным стенозом, стенозом ветвей легочной артерии. Подклапанный стеноз чаще является частью сложного ВПС. Препятствие оттоку крови из правого желудочка в легочную артерию обусловливает повышение систолического давления и гипертрофию правого желудочка. Величина градиента давления зависит от размера отверстия клапанного кольца. При СЛА легкой степени градиент давления между желудочком и легочной артерией составляет менее 30 мм рт. ст., при средней степени тяжести — 30—80 мм рт.ст., при тяжелой степени порока — более 80 мм рт.ст. У большинства детей до года и старше заболевание протекает бессимптомно, хотя в некоторых случаях отмечается небольшая утомляемость. Незначительный или умеренный СЛА может ничем не проявляться. При выраженном стенозе наблюдаются одышка, боли в сердце, бледность. Цианоз появляется в терминальной фазе. Границы сердца расширены в поперечнике. К характерным фи-зикальным данным относится систолическое дрожание в области верхней части левого края грудины и надгрудинной вырезки. Степень усиления правожелудочкового толчка нарастает по мере увеличения выраженности обструкции выходного отдела правого желудочка. Во втором межреберье слева от грудины выслушивается грубый систолический шум. Ослаблен II тон на легочной артерии, I тон на верхушке усилен. Имеется риск развития инфекционного эндокардита. Рентгенологически выявляется увеличение правых отделов сердца и легочной артерии (постстенотическое расширение) с обеднением легочного сосудистого рисунка. На ЭКГ определяются смещение электрической оси сердца вправо, гипертрофия правого желудочка и предсердия, блокада правой ножки пучка Гиса. С помощью допплеровского исследования (в том числе цветного картирования) оцениваются степень сужения, градиент давления между желудочком и легочной артерией и размеры камер сердца. Тетрада Фалло (ТФ) — самый частый синий порок сердца. ТФ характеризуется большим дефектом межжелудочковой перегородки, расположением аорты над местом дефекта, гипертрофией правого желудочка и стенозом легочной артерии. Вследствие больших размеров ДМЖП систолическое давление одинаково в обоих желудочках и аорте. Степень обструкции правого желудочка определяет направление и объем сброса крови. В большинстве случаев он достаточно велик, чтобы преодолеть системное сопротивление и вызвать сброс справа налево и развитие цианоза. Размеры ДМЖП имеют второстепенное значение, так как его диаметр в основном равен диаметру устья аорты. Различаются две основные формы ТФ. При крайнем варианте тетрады Фалло по типу общего ложного артериального ствола легочный ствол не работает, состояние ребенка тяжелое, наблюдается выраженное нарушение гемодинамики. Дети рано синеют, в 80 % случаев погибают на первом месяце жизни без оперативного вмешательства. При классическом варианте тетрады Фалло имеются стеноз легочной артерии (чаще клапанный и выхода из правого желудочка), дефект межжелудочковой перегородки (мембранозная часть), декстрапозиция аорты (аорта над дефектом межжелудочковой перегородки), вторичная гипертрофия правого желудочка. Цианоз у этих детей чаще возникает в 2—3-месячном возрасте, что обусловлено особенностями гемодинамики малого круга кровообращения. В то же время с рождения четко выслушивается систолический шум, обусловленный дефектом межжелудочковой перегородки, рано появляется одышка, часто у таких детей неправильно диагностируют дефект межжелудочковой перегородки и назначают дигоксин, который не показан при данном пороке. Дети отстают в физическом развитии, для них характерны одышка (при кормлении или движении ребенка), цианоз, деформация пальцев рук и ног («барабанные палочки»). Приступы усиливающегося цианоза с углублением дыхания — одышечно-цианотические — развиваются у детей до года и у детей младшего возраста. Границы сердца остаются нормальными или незначительно расширены влево. Вдоль левого края грудины выслушивается грубый систолический шум, II тон на легочной артерии ослаблен. У детей с ТФ могут наблюдаться тяжелая полици-темия или относительная анемия. Обструкция выносящего тракта правого желудочка прогрессирует. Прогноз неблагоприятный вследствие развития осложнений цианоза и полицитемии, таких как инсульт и абсцесс головного мозга. Часто развивается инфекционный эндокардит. Рентгенологически сосудистый рисунок легких обеднен, сердце небольших размеров, часто в форме «сапожка» с выраженной талией и приподнятой верхушкой. На ЭКГ выявляются смещение ЭОС вправо, гипертрофия правого желудочка и предсердия, часто блокада правой ножки пучка Гиса. Диагноз подтверждается данными эхокардиографии (возможна визуализация всех структурных компонентов тетрады Фалло, включая уровень обструкции выносящего тракта правого желудочка, цветное доп-плеровское исследование помогает установить направление сброса крови через дефект межжелудочковой перегородки), катетеризации сердца и ангиографии. 3. Врожденные пороки сердца с обеднением большого круга кровообращения. Коарктация аорты (К А). Сужение наблюдается ниже отхождения от аорты левой подключичной артерии. Хотя сужения могут локализоваться в любом участке, начиная от дуги и заканчивая бифуркацией аорты, в 98 % случаев они находятся в области ответвления артериального протока. При предуктивном стенозе (инфантильная форма) сужение наблюдается до ОАП, эта форма сочетается с другими пороками: ДМЖП, двустворчатым клапаном аорты, транспозицией магистральных сосудов и др. Постдуктивная форма (взрослая), при которой закрыт аортальный проток, имеет лучший прогноз. Артериальное давление над уровнем коарктации повышено. Определяется значительный градиент систолического давления между верхними и нижними конечностями. Наличие такого перепада давления ведет к компенсаторному развитию коллатеральных путей кровоснабжения нижней части туловища (обычно внутренняя грудная и межреберные артерии). Клинические проявления порока имеют место уже в период новорожденное. Симптомы у детей первого года жизни характерны для сердечной недостаточности. Часто отмечаются затруднения при кормлении и низкий прирост массы тела. У детей старшего возраста заболевание обычно протекает бессимптомно, хотя возможно наличие небольшой утомляемости или слабости в ногах при беге. Классическими признаками КА являются разные на руках и ногах пульс и артериальное давление: артериальная гипертензия на верхних конечностях и отсутствие или ослабление пульса на артериях ног и значительно более низкое АД на ногах, чем на руках (в норме на ногах АД на 10—20 мм рт. ст. выше, чем на руках). Выражена пульсация сосудов верхней половины тела, определяется приподнимающий левожелудочковый толчок. Границы сердца расширены влево. По левому краю грудины в 3-м и 4-м межреберных промежутках выслушивается систолический шум, распространяющийся на сосуды шеи и область спины. II тон на аорте усилен. Застойная сердечная недостаточность является самой частой проблемой у детей первого года жизни. Такие симптомы, как перемежающаяся хромота, головные боли, боль в груди, наблюдаются редко. На ЭКГ электрическая ось сердца смещена влево, выявляется гипертрофия левого желудочка. При рентгенографии определяются увеличение левых отделов сердца, восходящей и нисходящей аорты, узуры III—FV ребер в задних отделах. Эхокардиография позволяет лоцировать участок коарктации. Способствует подтверждению диагноза допплер-эхография с измерением градиента. При необходимости выполняется катетеризация сердца с проведением селективной левой вентрикулографии и аорто-графии. Аортальный стеноз (А С) составляет около 5 % от всех ВПС у детей. Чаще распространен клапанный стеноз (около 80 %), реже (20 %) встречаются подклапанный и надклапанный варианты аортального стеноза. Аномалия строения аортального клапана (двустворчатость) относится к основным врожденным порокам сердца у взрослых. Течение и прогноз порока определяются его локализацией и выраженностью, сочетанием с другими пороками сердца и фиброэластозом, сопутствующим поражением миокарда. Градиент систолического давления между левым желудочком и аортой во время изгнания крови прямо пропорционален квадрату величины кровотока. В зависимости от выраженности стеноза (градиент давления между желудочком и аортой) различат ются легкая (градиент давления меньше 50 мм рт. ст.), средняя (градиент давления 50—80 мм рт. ст.), тяжелая (градиент давления больше 80 мм рт. ст.) степень АС и критический стеноз — с острой сердечной недостаточностью в грудном возрасте. Симптоматика зависит от степени стеноза. При выраженном стенозе уже в грудном возрасте появляются признаки тяжелой левожелудочковой недостаточности, однако в большинстве случаев порок выявляется в школьном возрасте. Больные жалуются на утомляемость, одышку, боли в области сердца, головокружения, обморочные состояния. Цианоза не бывает. При пальпации области сердца определяются приподнимающий верхушечный толчок и систолическое дрожание во втором межреберье справа от грудины. Здесь же выслушивается грубый систолический шум, проводящийся на сосуды шеи. Брадикардия, максимальное и пульсовое давление низкое. Перкуторно и на рентгенограмме выявляется увеличение левых отделов сердца, на ЭКГ -левограмма, признаки гипертрофии левого желудочка и дистрофии миокарда. Степень выраженности стеноза устанавливается с помощью эхокардиографии (выявляются порок и степень гипертрофии левого желудочка, величина градиента давления на клапане и его дисфункция) и зондирования сердца. Приобретенные пороки сердца — приобретенные морфологические изменения клапанного аппарата, ведущие к нарушению его функции и гемодинамики. Чаще всего они возникают в результате перенесенного ревматизма, инфекционного эндокардита, системных заболеваний соединительной ткани, травмы, пролапса митрального клапана (ПМК). Основные признаки приобретенных пороков сердца приведены в таблице. Семиотика приобретенных пороков сердца
Недостаточность митрального (двустворчатого) клапана развивается при поражении его створок, а также подклапанного аппарата. Возникает как осложнение ревматизма, инфекционного эндокардита, системных заболеваний соединительной ткани, в результате травмы, ПМК, патологии клапанного аппарата: разрыва хорд, разрыва или дисфункции папиллярных мышц, дилатации митрального кольца или полости левого желудочка и др. Гемодинамика обусловлена ретроградным движением крови во время систолы левого желудочка в сторону предсердия, в связи с чем увеличивается кровенаполнение левого предсердия и левого желудочка. Вследствие дилатации и гипертрофии этих отделов сердца в аорту поступает необходимое количество крови, а часть ее возвращается обратно в левое предсердие. Жалоб дети могут не предъявлять. При длительно существующей недостаточности клапана может сформироваться выбухание левой половины грудной клетки — сердечный горб. Верхушечный толчок усилен и несколько смещен влево. Граница относительной сердечной тупости расширена влево. Прослушиваются ослабление тона на верхушке сердца, усиление II тона на легочной артерии и систолический шум с punctum maximum на верхушке сердца или в 5-й точке, который проводится к основанию сердца и в левую подмышечную область (реже на спину). Шум усиливается в положении ребенка на левом боку. На ЭКГ выявляются признаки гипертрофии левого предсердия и левого желудочка. При рентгенологическом исследовании обнаруживается увеличение левого желудочка и предсердия. На ЭхоКГ створки клапана во время систолы могут не смыкаться, выявляется увеличение размеров левого предсердия и левого желудочка. При допплер-эхокардиографии обнаруживается турбулентный поток крови в левое предсердие соответственно степени регургитации. Митральный стеноз может быть первичным (при латентно или подостро текущем ревматизме) или вторичным, возникающим на фоне недостаточности митрального клапана. Врожденный митральный стеноз проявляется сердечной недостаточностью в грудном и раннем детском возрасте. Давление в левом предсердии повышается, развивается его гипертрофия, ускоряется кровоток в левый желудочек из-за сужения митрального отверстия до 1 — 1,5 см2 (в норме площадь митрального отверстия 4—6 см2). Высок риск инфекционного эндокардита при любом поражении клапанов. При тяжелом митральном стенозе (площадь митрального отверстия <1 см2 давление в левом предсердии превышает 25 мм рт. ст., что приводит к легочной гипертензии и в покое. При развернутой клинической картине дети жалуются на одышку и быструю утомляемость (одышка при нагрузке возникает, когда площадь отверстия клапана уменьшается вдвое (< 2 см2). При осмотре выявляется бледность в сочетании со своеобразной окраской лица — цианотичным румянцем губ и щек (fades mitralis). Верхушечный толчок ослаблен, пальпируется «кошачье мурлыканье». Выслушиваются громкий и короткий («хлопающий») I тон и диасголический шум у верхушки сердца, который чаще слышен как пресистоли-ческий, но может быть и сочетанным, пресистолическим и протодиастолическим и просто мезодиастолическим. Определяются акцент II тона на легочной артерии, нередко его раздвоение или расщепление. При выраженной дилатации левого предсердия и легочной артерии возможны сдавление возвратного нерва и охриплость голоса (синдром Ортнера). Ортопноэ и ночные приступы сердечной астмы возникают при длительно существующем митральном стенозе, приводящем к легочной гипертензии и правожелудочковой недостаточности. Мерцательная аритмия, инфекции и инфекционный эндокардит могут при тяжелом митральном стенозе вызвать отек легких. На ЭКГ зубец Р вначале увеличен, затем становится двухвершинным. При рентгенологическом исследовании отмечается увеличение левого предсердия, на ЭхоКГ — однонаправленное движение передней и задней створок клапана вперед (в норме задняя створка в диастоле смещается кзади), снижение скорости раннего диастолического закрытия передней створки и амплитуды ее движения, утолщение клапана, расширение полости правого желудочка. Определяется сужение митрального отверстия до 1—1,5 см2 и более. Комбинированный митральный порок характеризуется доминированием клинических и инструментальных признаков одного типа порока, как правило митральной недостаточности в сочетании с менее яркими проявлениями стеноза отверстия (в частности, наличием типичного шума митрального стеноза над верхушкой сердца). Недостаточность аортального клапана. Чаще всего недостаточность аортального клапана возникает в результате деформации аортальных клапанов при ревматизме (почти всегда сочетается с поражением митрального клапана), вследствие инфекционного эндокардита, миксоматозной дегенерации клапанов, травмы, наследственных заболеваний соединительной ткани, врожденного двустворчатого клапана и др. При недостаточности аортального клапана часть крови возвращается во время диастолы из аорты в левый желудочек, в результате чего мышечные волокна левого желудочка растягиваются и гипертрофируются. Больные жалуются на одышку и сердцебиение, возникающие при физической нагрузке, нередко — на боли в области сердца. Кожные покровы бледные, нередко отмечается усиленная пульсация сонных артерий (пляска каротид). Пульс скорый и высокий, реже можно отметить появление капиллярного пульса. Артериальное давление характеризуется снижением минимального при нормальном или умеренно повышенном максимальном, причем степень снижения минимального давления пропорциональна степени недостаточности клапанов аорты. Верхушечный толчок при пальпации усилен и смещен кнаружи и вниз. Границы сердца расширены влево. На верхушке сердца выслушиваются ослабление I тона, на основании или, что более типично, в третьем-четвертом межреберье слева от грудины -протодиастолический шум. Шум, чаще тихий, нежный, льющийся, лучше выслушивается в положении больного стоя, при наклоне туловища вперед. Одновременно может выслушиваться и систолический шум (клапанное отверстие сужено относительно расширенных левого желудочка и аорты). Диастолический шум особого тембра (шум Флинта) выслушивается на верхушке сердца (обратный ток крови из аорты приподнимает опущенные в левый желудочек створки митрального клапана). На ЭКГ — признаки диастолической перегрузки левого желудочка. На рентгенограмме сердце имеет аортальную конфигурацию с подчеркнутой талией. На ЭхоКГ — створки аортального клапана не смыкаются. Могут выявляться вегетации на клапанах, косвенные признаки порока — дилатация левого желудочка и гиперкинез его створок. Допплеровское исследование позволяет выявить аортальную недостаточность и полуколичественно определить ее тяжесть (по ширине регургитирующей струи и глубине ее проникновения в левый желудочек, по времени обратного кровотока в грудной аорте и подключичных артериях). Стеноз устья аорты. Чаще всего стеноз устья аорты возникает в результате деформации и развития фиброза и кальциноза двустворчатого аортального клапана, вследствие перенесенного ревматизма (почти всегда сочетается с поражением митрального клапана), изолированного кальциноза аортальных клапанов, инфекционного эндокардита с массивными вегетациями, травмы. При стенозе устья аорты гемодинамика обусловлена сужением выходного тракта левого желудочка и увеличением нагрузки на левый желудочек (систолическая перегрузка). При легкой степени стеноза площадь отверстия аортального клапана равна 1,2—2 см2, при умеренном стенозе — 0,75—1,2 см2, при тяжелом стенозе <0,75 см2. 15—20 % больных при наличии симптомов стеноза аорты умирают внезапно. В фазе компенсации жалобы отсутствуют. Определяется систолическое дрожание на основании сердца. Во втором межреберье справа и в точке Боткина выслушивается систолический шум, скребущий, дующий, который проводится на сонные артерии. II тон на аорте ослаблен. Пульс малый, медленный, систолическое давление снижено. На ЭКГ — признаки гипертрофии левого желудочка. На ЭхоКГ при выраженном стенозе створки лоцируются как единый конгломерат эхо-сигнала, обнаруживается увеличение размеров левого желудочка. Допплер-эхокардиография выявляет турбулентный поток крови в аорту и позволяет с высокой точностью определить градиент давления между аортой и левым желудочком. Пролапс митрального клапана (ПМК) — это прогибание (пролабирование) митральных створок в полость левого предсердия во время систолы левого желудочка. Этот синдром чаще связан с аномалией строения клапана, при которой одна из его створок (чаще задняя) или обе провисают в конце систолы в полость левого предсердия. ПМК может быть первичным (идиопатическим) и вторичным (в результате врожденных или приобретенных заболеваний). Среди врожденных заболеваний ПМК чаще сочетается с наследственно обусловленными заболеваниями соединительной ткани (синдромы Марфана, Элерса-Данлоса, Холта-Орама и др.). У больных при этом часто наблюдаются астеническое телосложение, сколиоз, плоскостопие, вальгусная деформация стоп, расслабление связок. В возникновении ПМК определенную роль играет состояние подклапанного аппарата — удлинение или аномалии прикрепления хорд, форма створок клапана. ПМК возникает при патологических изменениях его створок и клапанных хорд, дисфункции папиллярных мышц, нарушениях сократимости левого желудочка при ревматизме, неревматическом кардите, бактериальном эндокардите, кардиомиопатиях, ВПС. ПМК часто сопутствует нейроциркуляторной дистонии и функциональной кардиопатии, при которых имеет место преобладание симпатического или парасимпатического отдела вегетативной нервной системы. В генезе его большую роль играет наследственная предрасположенность. Выделяются «аускультативная» и «немая» формы ПМК. Дети с ПМК особых жалоб не предъявляют, поэтому болезнь обычно выявляется случайно. Иногда отмечаются боли в сердце, головокружение, обмороки, что обусловлено вегетативными сдвигами, часто снижением АД. Основное клиническое проявление ПМК, выявляемое при аускультации, — мезосистолический щелчок на верхушке сердца, реже во втором-четвертом межреберьях слева у грудины, который может сочетаться с поздним систолическим шумом. Интенсивность шума варьирует по времени у одного и того же больного, шум и щелчок лучше выслушиваются в положении больного стоя. Иногда щелчок прослушивается как шум необычного тембра. При первичном пролапсе без регургитации на рентгенограммах грудной клетки размеры сердца нормальные, при вторичных они определяются характером основного заболевания. ЭКГ может не отличаться от нормы, однако для ПМК чаще характерны сниженные, двухфазные зубцы Т в отведениях II, III, AVF, V5,V6. Форма и величина зубца Г могут варьировать в зависимости от положения больного (в вертикальном положении ниже). При ЭхоКГ выявляется пролабирование одной или обеих створок. При «немом» ПМК на ЭКГ и рентгенограммах изменений не обнаруживается, он распознается только при эхокардиографии. Поделитесь этой записью или добавьте в закладки |
 Главная
Главная